产品分类
-
实验室仪器
按功能分按专业实验室分
- 化学合成
- 乳品类检测专用仪器
- 细胞工程类
- 种子检测专用仪器
- 病理设备
- 1. 乳品类检测专用仪器
- 1. 种子检测专用仪器
- 层析设备
- 动物实验设备
- 粮油检测
- 生物类基础仪器
- 植物土壤检测
- 1. 电泳(电源)仪、电泳槽
- 2. 分子杂交
- 3. 基因工程
- 4. PCR仪
- 5. 紫外仪、凝胶成像系统
- 药物检测分析
- 地质
- 纺织
- 分析仪器
- 农产品质量监测
- 1. 农药残毒快速检测仪
- 2. 农产品检测试纸
- 3. 农产品检测试药片
- 4. 土壤、化肥快速检测仪
- 5. 种子外观品质分析仪
- 水产品质量安全
- 水产技术推广
- 水生动物防疫
- 食品检测实验室
- 疾病预防控制中心
- 1. 快速检测试剂盒
- 2. 肉类检测仪器
- 3. 食品安全快速分析仪
- 4. 食品安全检测箱
- 5. 食品检测仪器配套设备
- 6. 食品安全检测仪器
- 7. 三十合一食品安全检测仪
- 8. 相关配置、配件
- 供水、水文监测
-
暂无数据,详情请致电:18819137158 谢谢!
-
暂无数据,详情请致电:18819137158 谢谢!
-
暂无数据,详情请致电:18819137158 谢谢!
-
暂无数据,详情请致电:18819137158 谢谢!
-
暂无数据,详情请致电:18819137158 谢谢!
-
暂无数据,详情请致电:18819137158 谢谢!
热销品牌 - 工业仪器
- 户外仪器
- 环境监测
- 便携式仪器
- 在线式仪器
为什么超纯水要即取即用?
[2017/6/16]
分析仪器(如HPLC、IC、AAS、ICP等)、细胞生物学、分析生物学、标准溶液和空白溶液配置、以及纳米材料科学等都会用到超纯水。大家知道自来水中含有千万种会影响科学实验结果的杂质,那么如何去除杂质,制造出“超纯水”?我们需要利用先进的技术来纯化水质。你知道吗?超纯水制造出来的瞬间,即刻开始与接触的环境产生溶解反应,我们可以戏称超纯水为“Hungry Water”,因为超纯水中溶解的离子浓度很低甚至没有, 这样极易会从外界环境中吸收杂质,如颗粒,挥发性有机物、细菌及其他污染物等,也可能从低级塑料和玻璃制造的储水器中吸收化学溶出物污染水质,还可以溶解空气中的二氧化碳,形成碳酸。
碳酸是一种弱酸,但由于超纯水中无任何主导型的相对强酸、强碱、共轭酸、共轭碱,碳酸就成为了唯一主导型的弱酸,也是唯一H+离子的来源(忽略掉H2O的解离)。
CO2(g)+H2O(l) ↹ H2CO3(l)
当超纯水开始曝露在大气下时,二氧化碳的溶解就会无可避免的持续下去,我们可以用电阻率的变化来监测这个过程。实践证明15MΩ.cm以上的超纯水暴露在空气中1个小时后水质就会下降至4MΩ.cm左右。
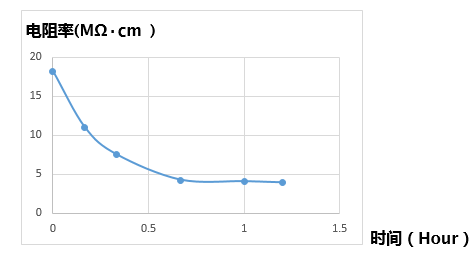
所以,超纯水最好能现场使用,任何方式的贮存或久放,除了会有容器本身造成的污染外,空气中的悬浮粉尘、挥发性有机物、微生物等污染及二氧化碳造成的电阻率下降,pH下降都是无法避免的。另外,久存的超纯水,TOC (总有机碳)及微生物也都有快速升高的隐忧,超纯水最好还是得即取即用。
下一篇:离心机使用过程中的注意事项介绍
























 河南、湖北、湖南、广东、广西、海南: 杨经理 19811942171 微信同号
河南、湖北、湖南、广东、广西、海南: 杨经理 19811942171 微信同号
 地址:广州市越秀区先烈中路76号15楼B、C
地址:广州市越秀区先烈中路76号15楼B、C 电话:020-37611206(20线)
电话:020-37611206(20线) 手机:13060606125
手机:13060606125  传真:020-37611206
传真:020-37611206 广州研发中心:广州市萝岗区科学城瑞发路1号
广州研发中心:广州市萝岗区科学城瑞发路1号


